谈谈胰十二指肠切除术(四)
七、胰十二指肠切除术的技术关键与技术改良
胰十二指肠切除术(Pancreaticoduodenectomy, PD)是治疗胰头、壶腹部及十二指肠恶性肿瘤的标准术式,但其技术复杂性高,涉及多脏器切除及复杂的消化道重建。自1935年由Whipple首次报道PD以来,死亡率已从40%降至<5%,但并发症如胰瘘(POPF)、出血和胃排空障碍仍显著影响预后[Cameron JL, et al.Current Surgical Therapy. 13th ed. Elsevier; 2020]。精准解剖与重建技术是降低并发症的核心。复杂胰头癌的PD往往手术难度更大,手术时间更长,相应手术并发症和手术死亡率更高。本文结合国内外最新研究,从手术入路、血管处理、消化道重建等方面简述PD的技术关键及技术改良,重点阐述了动脉优先入路和胰肠吻合技术,旨在为广大青年医生和医学生临床实践提供参考,为广大病员理解PD的复杂性提供一篇深度的医学科普。
(一)术前评估与手术规划
精确的术前评估和周密的手术规划对患者术后恢复至关重要。术前评估包括可切除性评估与手术安全性评估。
1、可切除性评估
主要是通过增强CT/MRI等影像学评估,联合三维重建,识别肝动脉变异(出现率15%-20%)、门静脉-肠系膜上静脉(PV-SMV)侵犯程度[Shrikhande SV, et al. Arterial variants in pancreaticoduodenectomy. HPB 2013;15(9):672-82],以及肿瘤和肠系膜上动脉或腹腔干的关系,评估肿瘤能否切除及是否需要血管切除与重建。
2、手术安全性评估
病人是否达到一般状况良好、心肺肝肾代偿功能正常、凝血功能正常的标准,并需评估脑血管情况和血栓风险以避免术中术后发生脑血管意外和血栓形成。一般状况中,营养风险评估尤为重要。对术前有营养风险的病人必须进行营养支持治疗,否则病人将更容易发生难以挽回的并发症。如有研究表明,术前血清白蛋白>3.0 g/dL可降低吻合口漏风险(OR=0.62, p<0.05)[Sandini M, et al. Prehabilitation in pancreas cancer.Ann Surg 2021;273(1):122-130]。
3、手术规划
决定治疗效果的四大基本要素是病人、病情、医生、医疗。因此,根据术前评估制定周密的手术规划,必须结合病人条件、医生团队技术实力与配合和医院设备设施,以安全、高效、精准、微创为原则合理选择开腹手术、腹腔镜手术或机器人手术,最重要的是最大限度地保证手术的安全性和有效性。
腹腔镜胰十二指肠切除术(LPD):在经验丰富的中心,手术时间可缩短至360±45分钟,出血量<200 mL[Palanivelu C, et al. Laparoscopic PD: 500 cases.Ann Surg 2022;275(2):e463-e469 ]。
机器人辅助胰十二指肠切除术(RPD):3D视野提高SMA周围淋巴结清扫完整性(R0切除率92% vs 开放手术89%)[Zureikat AH, et al. Robotic PD outcomes.JAMA Surg 2021;156(1):10-18]。
开腹手术:没有微创技术优势,但是最能保障手术安全的手术方式。在不适合行腹腔镜手术和机器人手术时应果断选择开腹手术;在腹腔镜手术或机器人手术中转开腹手术时,开腹手术是保障手术安全的最后一招。
(二)手术入路选择与动脉优先原则
传统PD多采用“由浅入深”的解剖顺序,但易因肿瘤侵犯血管导致术中出血风险增加。
胰头及壶腹周围肿瘤常侵犯肠系膜上动脉(SMA)及门静脉-肠系膜静脉轴(PV-SMV),传统PD术式因晚期发现血管侵犯而导致非治疗性开腹率高达15%-20%[ Pessaux P, Varma D, Arnaud JP.Pancreaticoduodenectomy: superior mesenteric artery first approach. J Gastrointest Surg. 2011;15(4):607-611]。动脉优先入路是胰十二指肠切除术的重大改良,特别是为LPD的开展提供有力的解剖入路支持。动脉优先入路通过早期解剖SMA及其分支,的现三大目标:(1)可切除性判断:明确肿瘤与SMA/腹腔干的关系,避免不可逆性血管损伤;(2)无瘤原则:优先离断动脉血供,减少术中肿瘤细胞播散;(3)钩突全系膜切除:沿SMA鞘膜锐性分离,确保淋巴脂肪组织整块切除[Kawabata Y, Hayashi H, Takai K, et al. Superior mesenteric artery-first approach in pancreatoduodenectomy: a systematic review and meta-analysis. J Hepatobiliary Pancreat Sci. 2020;27(3):103-113]。
1、动脉优先入路的解剖学基础
(1)SMA的解剖变异与手术风险
SMA起始部:通常位于腹腔干下方1-2cm,但约12%患者存在高位起源(与腹腔干共干),增加术中误伤风险[Nimura Y, Nagino M, Takao S, et al. Standard versus extended lymphadenectomy in radical pancreatoduodenectomy for ductal adenocarcinoma of the head of the pancreas. J Hepatobiliary Pancreat Sci. 2012;19(3):215-222]
胰十二指肠下动脉(IPDA):80%源自SMA右前壁,距离起始部1.5-3.0cm,早期结扎可减少钩突分离时出血[Hackert T, Strobel O, Michalski CW, et al. The TRIANGLE operation – radical surgery after neoadjuvant treatment for advanced pancreatic cancer: a single arm prospective study. HPB (Oxford). 2017;19(11):1001-1008]
异位肝右动脉:8%-15%起源于SMA,术中误扎可导致肝右叶梗死[Sanjay P, Takaori K, Govil S, et al. 'Artery-first' approaches to pancreatoduodenectomy. Br J Surg. 2012;99(8):1027-1035]
(2)钩突系膜与SMA鞘膜的淋巴引流
“系膜三角”概念:钩突系膜包含胰头神经丛、淋巴管及IPDA,是胰腺癌局部扩散的主要路径;
SMA鞘膜清扫:有人报道,完全切除SMA右侧180°鞘膜,使淋巴结阳性率从35%降至18%。
2、动脉优先入路与关键技术
目前,报道至少有六种动脉优先入路应用于PD特别是LPD,分别是右后方入路(P)、中部钩突入路(R)、横结肠系膜下入路(M)、左后方入路(L)、前入路(A)和上入路(S),如下图。其核心是在没有处理肠系膜上静脉(SMV)和门静脉(PV)系统之前优先探查或离断SMA系统和CA与钩突的连接(动脉优先入路示意图均来源于丁香园)。
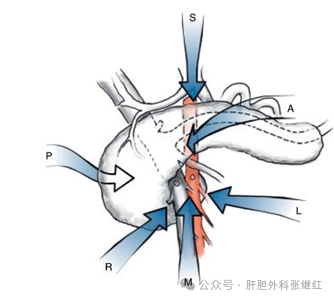
在本文前面已经介绍过动静脉入路,本文着重介绍动脉优先入路的基本方法和技术关键。
(1)后方入路(Posterior Approach)(Kocher入路)
适应证:优先探查SMA和腹腔干受侵犯情况,适用于胰头颈部后内侧肿瘤、壶腹周围癌或胰头非钩突无血管侵犯小肿瘤。
技术关键:通过Kocher手法充分游离胰头后部,显露SMA右侧缘,优先结扎胰十二指肠下动脉(IPDA);沿SMA右侧180°分离鞘膜,确保钩突系膜整块切除;避免损伤SMA后方交感神经丛,减少术后腹泻。
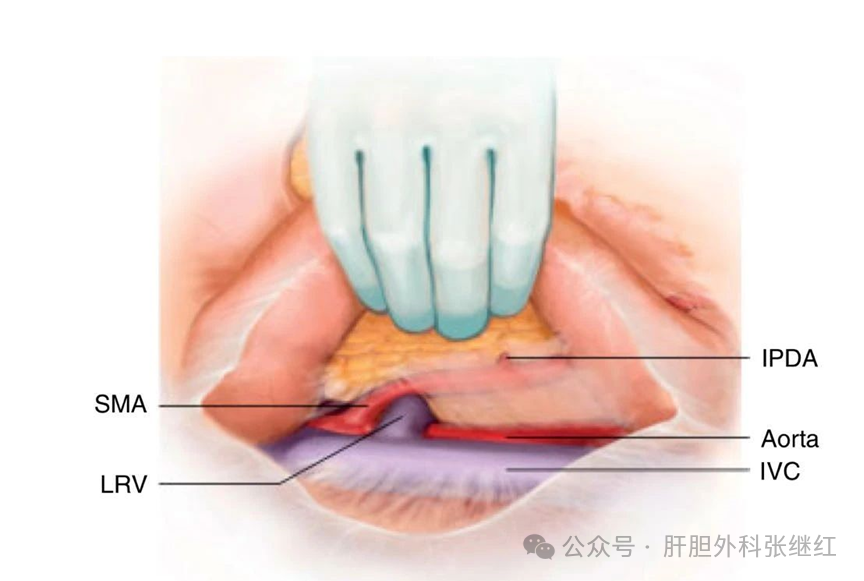
优势:有效R0切除率提升,减少术中出血量。
(2)上方入路(Superior Approach)
适应证:肿瘤侵犯CHA或腹腔干。
技术关键:解剖肝总动脉(CHA),优先离断胃十二指肠动脉(GDA),显露SMA起始部;暴露腹腔干,沿CHA向腹腔干方向分离,明确肿瘤与腹腔干和肠系膜上动脉的关系。
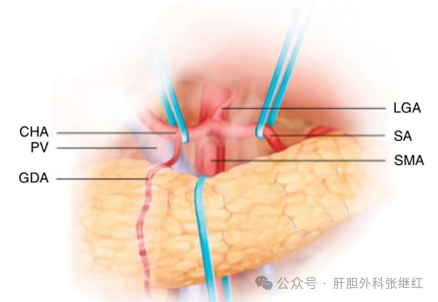
优势:避免肿瘤残留于CHA周围,降低局部复发率。
(3)左侧入路(Left Posterior Approach)(Treitz韧带入路)
适应证:钩突或腹侧胰腺肿瘤。
技术关键:牵拉近端空肠以显露SMA后侧和右侧。切断treitz韧带,向左侧牵拉近端空肠;从SMA起始处分开第一支空肠动脉;进一步牵拉空肠使SMA逆时针旋转,便于识别和分离IPDA。
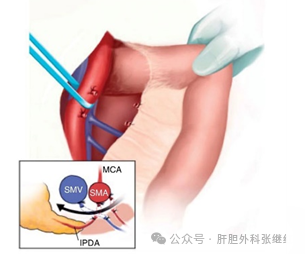
还有一种左后下侧入路的技术关键:是从小肠系膜开始完成肠系膜上动、静脉的探查。将小肠系膜完全游离并向头侧翻转,然后于SMA根部右侧分离找到并分离SMV;再于SMV左侧分离找到SMA。
优势:在不游离十二指肠和结肠的情况下充分游离SMA后侧和右侧,提高R0切除率 。
(4)前方入路(Anterior Approach)
适应证:胰头上部肿瘤。
技术关键:切开胰颈部以暴露SMV/PV。通过结肠中静脉定位SMV,显露SMA前壁,实现SMV-SMA夹角分离。IPDA早期结扎:减少钩突分离时出血。
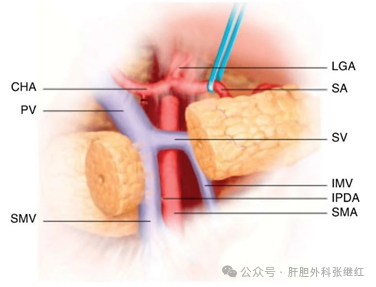
优势:术中出血量减少,快速控制IPDA。
(5)钩突优先入路(Uncinate Process-First Approach)
适应证:钩突肿瘤(侵犯SMV或SMA分支)。
技术关键::优先离断胰颈,显露SMV主干。自胰颈断端经钩突分离SMV,解剖SMV第一空肠支、SMA,将钩突从SMA尾侧剥离,确保完整切除。
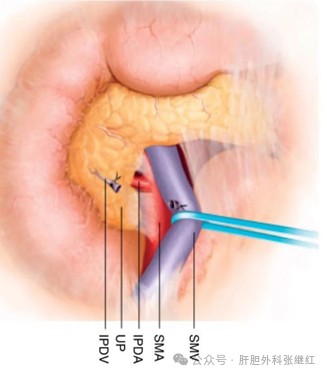
优势:局部复发率降低。
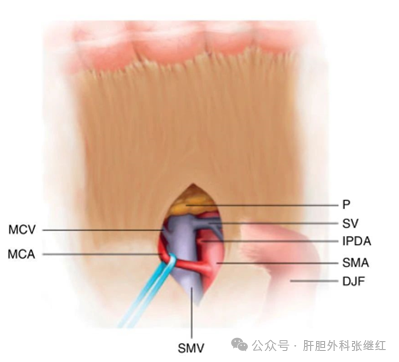
(6)横结肠系膜下入路
适应症:钩突部肿瘤。
技术关键:结肠下区小肠系膜根部打开浆膜,利用该区的空间优势,逐步分离显露SMA至腹主动脉发出根部,分离结扎第1支空肠动脉及胰十二指肠下动脉,同时将SMA逐步与肿瘤分离并骨骼化,切除SMA右侧淋巴组织以及空肠第1支动脉附近的淋巴结。
优势:SMA根部是胰腺癌转移的重要部位,在充分游离SMA后清除SMA根部周围淋巴与软组织会更加安全、彻底,实现肿瘤根治性切除,改善长期预后。
具体选择什么入路,要根据术前三维重建(CTA/MRI)及术中探查结果动态调整入路。不能一条路都到黑!
(三)血管处理与淋巴结清扫
1、血管处理技术
(1)肝总动脉(CHA)或右肝动脉变异时(如起源于SMA),要优先保留变异的肝动脉,如为肿瘤侵犯需优先重建肝动脉血供,以避免术后肝脏缺血性梗死甚至导致肝功能衰竭。
(2)肠系膜上动脉(SMA)右侧切除胰腺系膜
处理胰十二指肠下动脉(IPDA)时要注意保留至空肠第一动脉分支,降低缺血性肠炎风险[Nakamura M, et al. Mesopancreas dissection in PD.J Gastrointest Surg 2021;25(7):1873-1881]。
(3)解剖显露门静脉及肠系膜上静脉
针对胰头复杂解剖,环血管技术(circumvascular technique)通过系统性分离血管周围组织,实现更彻底的淋巴结清扫和血管保护,尤其适用于侵犯门静脉(PV)或肠系膜上静脉(SMV)的病例。
当肿瘤侵犯PV/SMV时,需联合血管切除并重建。PV/SMV受累<180°可行楔形切除,>180°需节段切除+端端吻合(5年生存率无显著差异)[Zhou Y, et al. Vascular resection in PD. Ann Surg 2019;270(5):883-891]。
根据侵犯长度,可采用直接端端吻合(≤3 cm)或自体血管或人工血管移植,需要血管移植时应优先选择自体血管移植。有报道,自体颈内静脉移植血栓发生低于人工血管移植(血栓率8% vs 人工血管25%)[Kleive D, et al. Vascular grafts in PD. Br J Surg 2020;107(1):69-78]。术中需控制血流阻断时间(<60分钟),以减少肠道淤血及术后肝功能损伤。
2、淋巴结清扫
淋巴结清扫范围:根治性PD要求彻底清扫肝十二指肠韧带、腹腔动脉干及肠系膜上动脉周围淋巴结,并骨骼化处理肝动脉、门静脉等大血管,避免遗漏转移灶。
(三) 消化道重建技术
消化道重建策略:采用Child法顺序(胰肠-胆肠-胃肠),减少胆汁激活胰酶,理论上可降低胰瘘风险。
1、胰肠吻合基本方式
胰瘘是PD术后最常见并发症(发生率10%-20%),其风险与胰腺质地、胰管直径及吻合技术密切相关。胰肠吻合的基本方法有两种:
(1)胰管-空肠黏膜对黏膜吻合
该技术强调胰管与空肠黏膜的直接吻合,适用于胰管直径≥3 mm的患者,需支架管支撑。其核心在于确保胰管与肠黏膜的连续性,减少胰液渗漏。研究显示,胰管-空肠黏膜对黏膜吻合可维持胰管通畅性并保护外分泌功能,但技术要求高,胰管过细或胰腺质地软时易失败。
一般需缝合两层,先缝合胰腺断端后壁与空肠浆肌层,在空肠上开一小口,将胰管与空肠黏膜对黏膜缝合,最后缝合胰腺断端前壁与浆肌层。
(2)套入式吻合
将胰腺残端套入空肠,适用于胰管细小者。
①胰肠端端套入式吻合
该术式通过将胰腺断端套入空肠腔内完成吻合,适用于胰腺直径较小、胰管无明显扩张的患者。操作要点包括:游离胰腺断端2-3 cm,空肠后壁浆肌层与胰腺后壁间断缝合,胰管内置入引流管,最后将空肠前壁与胰腺前壁缝合固定。但其缺点显著,如胰腺断端暴露于肠腔易被胰液腐蚀,套入困难时易致组织撕裂,且愈合时间较长。
②胰肠端侧套入式吻合
适用于胰体宽厚、胰管不扩张的患者。通过关闭空肠断端并在系膜对侧缘切开,完成胰腺与空肠的侧壁吻合。其优势在于减少吻合张力,但对空肠肠腔较大或胰腺狭窄者操作难度较高。
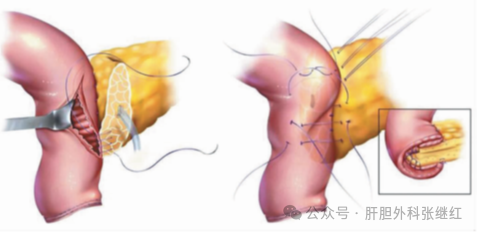
该图来源于《外科理论与实践》
2、胰肠吻合改良术式
从上表可见三种吻合方式均不可避免胰瘘发生。为尽可能避免胰瘘的发生,无数医学前辈做了大量技术改良,创建了很多切实可行的技术方法,特别是针对腹腔镜下胰肠吻合做了大量改进,取得一定效果。
(1)胰管空肠黏膜对黏膜吻合改良术式
①Blumgart胰肠吻合
A:胰管两侧以双针分别贯穿缝合胰腺断端及空肠后壁浆肌层;B:间断缝合胰管与空肠壁全层;C:以双针分别缝合空肠壁浆肌层前壁;D:打结,使肠壁浆肌层覆盖于胰腺断端。
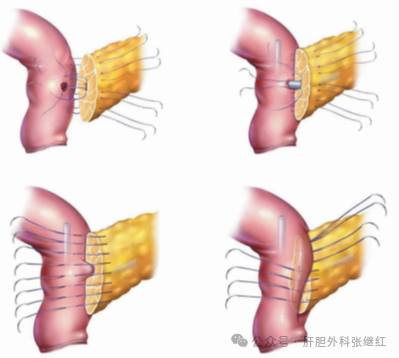
该图来源于《外科理论与实践》
② 一针法
洪德飞等基于对“胰管支架”应为“胰液引流管”和黏连愈合的理念认识,提出了腹腔镜PD中应用“一针法”进行胰肠吻合。主要的技术关键包括:A 选取匹配胰管直径的胰液引流管。B 一针贯穿胰管腹侧、胰液引流管前后壁及胰管背侧,打结妥善固定引流管。C 空肠切口荷包全层缝合并适当收紧,保留胰腺断端和空肠靠拢余地的同时避免肠液流出空肠切口。D 利用胰腺断端和空肠浆肌层的缝合拉拢胰管和空肠。
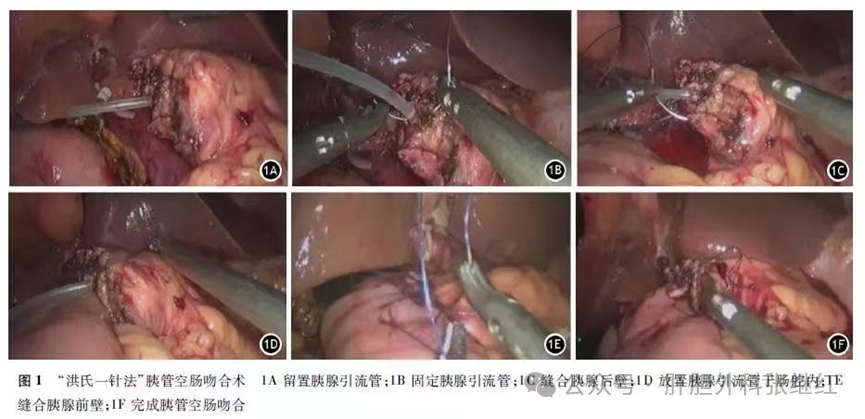
来源于《中华胰腺病杂志》
③一针法结合陈氏缝合技术应用于胰肠吻合
一针法贯穿固定胰管引流管,然后应用连续U型贯穿缝合法包埋胰腺残端。
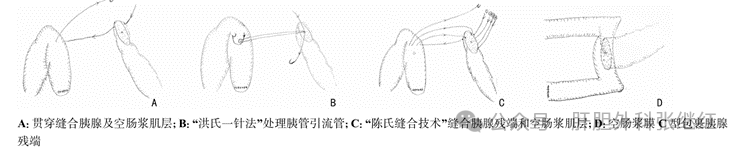
来源于《中国肿瘤临床杂志》
④Kakita法
本质上是先行胰管空肠黏膜吻合,然后贯穿胰腺全层和空肠浆肌层将胰腺残端包埋于空肠壁。即:先于空肠侧壁做一与主胰管直径相同的小切口,然后将置入引流管的主胰管与空肠行全层吻合,再用穿过胰腺全层和空肠浆肌层的缝线行第二层吻合。
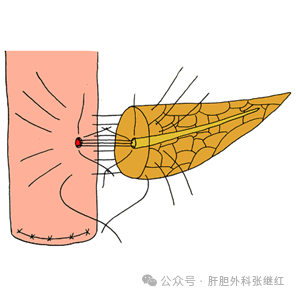
该术式对胰管-空肠黏膜吻合的外层缝合进行简化,由胰腺前被膜贯穿胰腺全层至后被膜,直接以较大针距横向缝合空肠浆肌层,间断缝合并打结,使胰腺断端与空肠浆肌层紧密贴合。该法适于各种胰腺质地和胰管直径的病人。
⑤双针法
先在空肠打孔处预置荷包缝合线。胰肠吻合按照先背侧、后腹侧“两层”连续缝合的思路进行,头侧和足侧分别打结。①背侧吻合:在胰腺下缘相对应处空肠侧缝合,打孔处层面进针,在其背侧约2 cm处出针;胰腺断端由背侧向腹侧走针,胰管层面胰腺组织出针,完成第一针缝合,遵此“空肠侧进针,胰腺侧出针”顺利完成胰肠吻合背侧层,根据胰腺宽厚程度一般需要4~5针,最后一针于胰腺断端由背侧向腹侧走针,胰腺腹侧出针,预备和腹侧缝线打结。②插管:胰腺支撑管插入空肠打孔处,收紧预置荷包缝合线。③腹侧吻合:助手夹取双针线另一针进入体内,于胰腺下缘胰腺断端由腹侧向背侧走针,胰管层面胰腺组织出针,空肠打孔处层面进针,在其腹侧约2 cm处出针,完成第一针缝合,遵此“胰腺侧进针,空肠侧出针”顺利完成胰肠吻合腹侧层,针数和背侧吻合相同,最后一针于空肠侧由打孔层面向腹侧走针。④血管线两端的针剪掉后于胰肠吻合头侧打结;将胰肠吻合口足侧剩余血管线裁剪至合适长度,用力均匀缓慢收紧,避免切割胰腺组织,打结完成胰肠吻合[洪德飞,刘亚辉,刘建华,等.腹腔镜胰肠吻合技术[J]. 中国实用外科杂志,2022,42(5):539-549]。
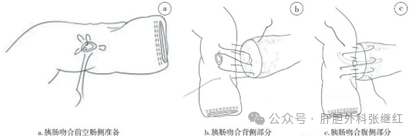
来源于《中国实用外科杂志》
⑥一层缝合法
对于胰管较粗的病人,可一层缝合:胰腺断端腹侧的脏层腹膜面进针,胰管内出针,空肠黏膜面进针,浆膜面出针。可间断,可连续。如苗教授单针prolene自胰腺断端腹侧的脏层腹膜面进针,胰管内出针,空肠黏膜面进针,浆膜面出针,类似于“车轮状”、“螺旋样”连续缝合,自头侧向足侧先吻合后壁,而后自头侧向足侧再吻合前壁,于胰肠吻合口足侧打结缝合,此吻合使用1针1结,1层吻合。
(2)套入式吻合的改良术式
①捆绑式吻合
彭淑牖教授创建了一种捆绑式吻合技术,尤其适用于胰管不可见的病例。捆绑式胰肠吻合目的是达到使吻合口处无针孔针道与腹腔环境直接相连,针距间空隙及空肠胰腺间空隙彻底消失的效果,以降低胰瘘发生率。
技术关键:胰腺断端游离约3 cm;空肠断端向外翻转3 cm,用电凝或石炭酸破坏外翻肠袢的黏膜,使其失活;再将空肠和胰腺断端靠拢,行胰腺断端与空肠黏膜连续或间断缝合(要求仅缝合空肠黏膜,避免穿透浆肌层);然后将黏膜面已破坏的空肠浆肌鞘翻回原状,胰腺断端自然进入肠腔内,然后将空肠断端与胰腺被膜间断缝合固定;最后在接近空肠断端 1.5~2.0 cm,两条系膜动脉之间以缝线环绕空肠结扎,使空肠与胰腺紧密相贴完成捆绑。
捆绑式胰肠吻合适用于胰瘘高风险的胰管狭窄和胰腺柔软的病例。其技术难点在于对胰腺的充分游离(3 cm)和捆绑线松紧的把握,捆绑过松容易在吻合口留下缝隙,过紧则可能影响吻合口血供并引起切割损伤。过粗的胰腺残端是其禁忌证。
②“U”形贯穿缝合(陈式胰肠吻合法)
陈孝平院士通过全层贯穿胰腺实质和肠壁的间断交锁“U”型缝合或者连续缝合,将胰腺断端的主胰管、副胰管、小叶导管引流的胰液全部引流入肠腔内无遗漏。即:通过2~4根贯穿肠壁与胰腺的“U”形缝线将胰腺残端收紧并插入肠腔,再予空肠浆肌层与胰腺包膜间断缝合数针[颜伟康,刘颖斌. 胰肠吻合方式发展历史与现状[J]. 中国实用外科杂志,2022,42(4):464-467]。
③荷包式胰肠端端吻合
1994年,Spivack等首次提出荷包式胰肠端端吻合,这一手术方式的特点是应用空肠吻合口末端全层的荷包缝合环扎空肠及胰腺,取代了胰腺包膜与空肠吻合口间断缝合。 在胰腺手术中引入了吻合口荷包缝合的概念[颜伟康,刘颖斌. 胰肠吻合方式发展历史与现状[J]. 中国实用外科杂志,2022,42(4):464-467]。
④荷包式胰肠端侧吻合
荷包式胰肠端侧吻合是将空肠侧壁切开吻合口后埋置荷包形缝合线,将胰腺残端埋入空肠并行加固。有学者使用3根缝线的荷包式胰肠端侧吻合方法,1根荷包缝合线预置于空肠吻合口周围的浆肌层内,2根“U”形缝线将胰腺残端拉入并褥式缝合固定于肠腔内,然后行荷包缝合线打结环紧胰腺[颜伟康,刘颖斌. 胰肠吻合方式发展历史与现状[J]. 中国实用外科杂志,2022,42(4):464-467]。
该术式仍适用于柔软胰腺的胰肠吻合。荷包式胰肠端侧吻合仍存在收紧荷包线的松紧把握问题,过紧还可能压迫闭塞较狭窄的胰管。
⑤捆绑式胰肠端侧吻合
将胰腺断端与肠吻合口内壁缝合套入后,利用预置于肠壁浆肌层的荷包缝合线行捆绑,将与胰腺相通的针孔封闭限制于肠内。
该术式的优势在于能够处理端端捆绑时无法套入的过粗残端,同时通过适当规划空肠吻合口大小,能够使肠管平滑肌收缩时卡住胰腺残端。但有术后肠袢压力过高导致的吻合口撕裂的风险,说明该术式需要对肠袢充分减压[颜伟康,刘颖斌. 胰肠吻合方式发展历史与现状[J]. 中国实用外科杂志,2022,42(4):464-467]。
⑥鲨嘴式胰肠端侧吻合
垂直空肠走行方向切开空肠后壁后,将胰腺断端后壁与空肠切口远端浆肌层间断缝合,胰腺断端前壁与空肠切口近端浆肌层间断缝合,最后将近端空肠间断缝合于胰腺前壁包膜,使近端空肠覆盖于胰腺前壁[洪德飞,刘亚辉,刘建华,等. 腹腔镜胰肠吻合技术[J].中国实用外科杂志,2022,42(5):539-549]。
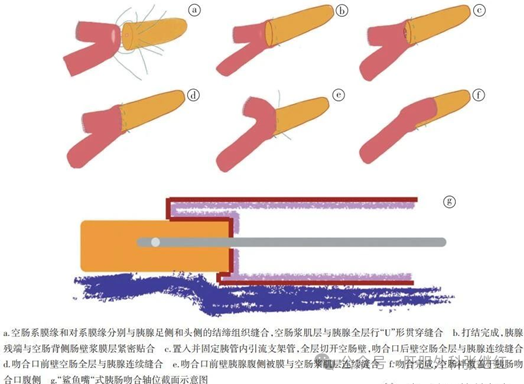
来源于《中国实用外科杂志》
该术式对胰腺残端粗细并无多少限制,适合较大或柔软的胰腺残端的吻合。
理论上导管对黏膜的胰肠吻合胰瘘发生率相对较低。至于到底哪种吻合方法胰瘘的发生率较低,没有共识。实践中,手术者最熟悉那种方法就用哪种方法吻合,这样可能有利于降低胰瘘发生率。胰管直径、胰腺质地(软/硬)及术者经验是关键影响因素,术式选择需个体化。胰管扩张(≥3 mm)优先选择胰管空肠黏膜吻合或改良端侧吻合。胰管细小或胰腺质地软选择套入加捆绑式或“荷包背带裤式”更安全。 腹腔镜手术采用改良Blumgart法或“荷包背带裤式”因操作便捷,更适合微创手术。
3、胆肠与胃肠吻合
胆肠吻合多采用端侧吻合(技术关键及技术改良详见本公众号文章“胆肠吻合的手术原理与应用要点”),位置需距离胰肠吻合口5-10 cm以减少反流性胰腺炎。
胃肠吻合则推荐结肠后位,采用机械吻合或手工缝合。
PD的成功依赖于精准的血管处理、个体化吻合技术及多学科协作。
