谈谈胰十二指肠切除术(三)
六、腹腔镜胰十二指肠切除术
腹腔镜胰十二指肠切除术(LPD)就是利用腹腔镜手术技术完成或辅助完成的胰十二指肠切除术。包括全腹腔镜胰十二指肠切除术、腹腔镜辅助胰十二指肠切除术和和腹腔镜机器人联合手术。腹腔镜辅助胰十二指肠切除术包括在腹腔镜下完成胰十二指肠切除、通过腹壁小切口完成消化道重建手术和手助腹腔镜胰十二指肠切除术(通过上腹部小切口将手伸入腹腔内协助完成手术)。腹腔镜机器人联合手术是在腹腔镜下利用机器人完成胰十二指肠切除和消化道重建全过程。
(一)腹腔镜胰十二指肠切除术的适应证
同开腹胰十二指肠切除术。
(二)腹腔镜胰十二指肠切除术的禁忌证
1、绝对禁忌证
(1)开腹手术禁忌证;
(2)不能耐受气腹或无法建立气腹者;
(3)腹腔内广泛粘连及其他原因难以显露、分离病灶者;
(4)腹腔镜下无法满足无瘤技术原则(整块切除、无接触、肿瘤供应血管阻断)者。
2、相对禁忌证
(1)病灶紧贴或直接侵犯胰头周围大血管需行大范围血管切除置换者;
(2)病变过大,影响器官和重要组织结构的显露,无法安全行腹腔镜下操作者;
(3)超大体重指数影响腹腔镜操作者。
(三)腹腔镜胰十二指肠切除术的手术入路
其实腹腔镜手术入路与传统开腹手术可以相同,但腹腔镜从前向后、从下向上、从左到右和从右向左均具有视觉上的优势,因此,手术入路较开腹手术更加灵活多样。LPD在处理胰头钩突时,围绕肠系膜上血管轴可将入路大致分为三类:静脉入路、动脉入路和动静脉混合入路,即以PV-SMV为中心的静脉入路、以SMA为中心的动脉入路和动静脉入路交叉进行的混合入路。
1、静脉入路
静脉入路是沿用开放胰十二指肠切除术最常用的标准入路方式,其钩突的切除围绕PV-SMV轴展开。
综合文献观点,从右向左开始的经典Kocher入路:首先打开胃结肠韧带,然后离断肝结肠韧带。游离结肠右半部与胰头十二指肠前方,并离断Henle干,随后以Kocher切口显露下腔静脉、腹主动脉、腹腔干、左肾静脉及肠系膜上动脉等。肿瘤无PV-SMV侵犯,如神经内分泌肿瘤、低度恶性肿瘤以及十二指肠乳头癌、壶腹部癌、胆管下段癌等,同时术前判断也不存在SMA周围淋巴结转移情况的病人,行常规静脉入路即可。
2、动脉入路
以肠系膜上动脉轴为中心分为前、后、左、右四条基本入路,在此基础上可演变为至少六种以上入路(下图来源于《中国实用外科杂志》)。对于肿瘤侵犯PV-SMV和肿瘤可能已经累及SMA但术前判断仍可切除,如临界可切除胰头癌,建议优先选择动脉入路。
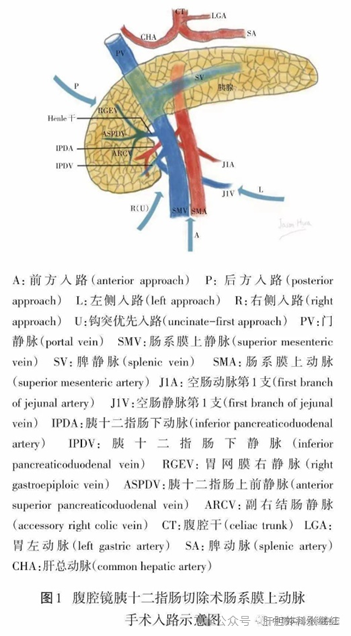
(1)SMA前方入路
此入路从结肠上区或结肠下区由SMA发出的结肠中动脉根部起始,沿SMA由下至上、由浅入深清淋巴脂肪组织扫至腹腔干起始部右侧。要点是离断胃和胰颈,悬吊SMV向右侧牵引直接解剖显露SMA并处理钩突。
(2)SMA后方入路
Kocher切口显露下腔静脉、左肾静脉,于左肾静脉上方腹主动脉前显露肠系膜上动脉,根据情况决定是否显露SMA。
(3)SMA左侧入路
该入路为结肠下区沿SMA左侧的入路方式,部分学者亦称之为SMA左后入路。要点是结肠下区Treitz韧带入路离断空肠,游离近端空肠系膜并将近端空肠向左牵拉以使SMA逆时针转位,然后处理钩突。这时位于SMA后方的空肠动脉第1支与IPDA的共同干根部以及右侧的IPDA被牵至左侧,以便于环SMA处理;将SMA向右前牵拉并继续向左牵拉近端空肠,SMV则被牵至SMA后方。
(4)SMA右侧入路
SMA右侧入路亦即钩突内侧入路(medial uncinate approach)或钩突优先入路(uncinate-first approach)。要点是Treitz韧带入路离断空肠,将十二指肠及近端空肠自肠系膜血管后方牵至右侧,悬吊SMV并向左前方牵引,使SMA顺时针转位,便可在SMV下方显露并处理钩突。
3、动静脉混合入路
动静脉混合入路即采取动脉入路和静脉入路结合的入路方式。这种入路方式通常先探查胰颈上、下缘,初步判断PV-SMV及肝动脉受侵情况,接着从动脉入路判断SMA有无受侵,根据探查情况再行后续操作,通常先沿SMA动脉入路分离,再结合SMV静脉显露,分别将SMA及SMV悬吊,将血管与胰头钩突完全分离。动静脉混合入路的变种有很多,其优势在于同时保留了动脉入路和静脉入路的优点。这种方式改良的方法很多很灵活,比如有作者提出的“前入路静脉优先与右后入路动脉优先”、“横结肠系膜下方的动静脉混合入路”等。
(四)腹腔镜胰十二指肠切除术的基本流程
腹腔镜胰十二指肠切除术(LPD)和机器人胰十二指肠切除术(RPD)是高科技带来的产物,其核心理念和技术与OPD是一致的,都是开腹手术和经验的传承。一个具有丰富开腹腹腔镜胰十二指肠切除术经验的专家,有助于他顺利开展LPD或RPD。技术平台不一样,但都是一个技术复杂、需要团队密切配合完成的高难度、高风险手术。
腹腔镜手术和开腹手术在手术时间、术中出血量、术后并发症、围手术期死亡率、淋巴结清扫数目、总生存期和无瘤生存期均无显著差异,还具有微创技术优势,但设备和技术要求高于开腹手术。手术操作主要步骤与开腹手术是一致的,但手术入路和操作流程有所不同。
布孔原则:便于操作、便于显露,常用五孔法(下图来源于《腹腔镜胰十二指肠切除手术专家共识2017)》)。
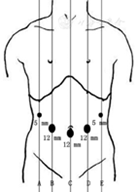
手术流程:利用腹腔镜视觉,以门静脉-肠系膜上静脉为轴线,采取静脉优先的途径;或者以肠系膜上动脉为轴线,采取动脉优先途径;从左向右、从前向后、从足侧向头侧的顺序进行切除。
根据有关文献和临床经验,腹腔镜手术可以依据不同入路,解剖显露可采取从胰头十二指肠结合部后方、上方、前方的顺序,或者从后方、下方、上方的顺序进行切除,以胰、胆、胃的顺序和空肠进行吻合重建。
普及腹腔镜手术的第一难点在于胰肠吻合(详见本公众号文章《谈谈胰十二指肠切除术(四)》之七、胰十二指肠切除术的技术关键与技术改良)。胰肠吻合基本方式有胰管空肠吻合和胰腺空肠导入式吻合。完美的胰管空肠吻合术要求粘膜对粘膜吻合,在开腹状态下较容易完成且技术成熟,但在腹腔镜下不仅时间长且很难高质量完成。为此,学界做了许多探索和改良。但机器人辅助下的腹腔镜胰十二指肠切除术可以较完美进行胰肠吻合。
吻合口愈合机理有生长性愈合和粘连性愈合。生长性愈合是组织胚胎来源一致,血供丰富,针距、边距理想,对合准确,只要患者营养良好,愈合迅速。粘连性愈合是组织胚胎来源不一致,血供较差,愈合过程缓慢,如瘘管、窦道。胰管空肠吻合术在胰管较粗的情况下可以达到生长性愈合,但在胰管细小时,即使开腹手术难以实现口对口(粘膜对粘膜)的理想吻合,在腹腔镜和机器人辅助下更难完成理想胰管空肠吻合,这时主要依赖于空肠浆肌层与胰腺断端的粘连性愈合;或者行套入式胰肠吻合实现空肠浆肌层与胰腺被膜的粘连性愈合。有学者以“人工瘘管”学说简化了胰管空肠吻合技术,以引流胰液+简单组织对合替代了粘膜对粘膜的胰管空肠吻合术,其愈合机理主要依赖于粘连性愈合,这一学说的实际运用,简化了开腹、腹腔镜、机器人胰肠吻合技术,为普及腹腔镜胰十二指肠切除术奠定了基础。
其次是胆肠吻合。开腹手术时可以间断缝合,完成粘膜对粘膜的全层缝合。腹腔镜下胆肠吻合很难全部间断缝合,一般采取后壁连续前壁间断的缝合方法,或者全部连续缝合的方法进行胆肠吻合。这种吻合技术,在胆管较粗的病例可以保安证吻合质量,术后吻合口并发症发生较少;但在胆管口径较小的病例,临床上发生吻合口狭窄的病例并不少见。因此,手术者应根据自身经验和技术选择缝合技术(详见本公众号文章《胆肠吻合的手术原理与应用要点》)。
依据2017年《腹腔镜胰十二指肠切除手术专家共识》,腹腔镜胰十二指肠切除术的主要步骤如下:
(1)Kocher切口
切开胃结肠韧带后,根据术者习惯和肿瘤情况合理选择传统Kocher切口或反向Kocher切口路径和是否采用动脉入路。传统Kocher切口遵循开腹胰十二指肠切除术方法,沿右肾前筋膜、十二指肠第2段、胰头后方路径向左侧游离至腹主动脉左侧缘。
根据术者习惯及肿瘤情况,可选择是否优先探查、游离、悬吊肠系膜上动脉;清扫肠系膜上动脉右侧180°淋巴结;夹闭或结扎、离断胰十二指肠下动脉。探查腹腔干根部,从其根部向肝动脉、脾动脉方向清扫淋巴结。
反向Kocher切口则是在离断空肠后,沿空肠和屈氏韧带后方分离十二指肠第2、3段和胰头后方的疏松结缔组织,直达十二指肠降部外侧缘。
(2)离断胃或十二指肠
保留幽门或不保留幽门LPD的胃离断处理方法均同开腹胰十二指肠切除术。保留幽门LPD应在距幽门至少2 cm位置离断十二指肠。保留幽门LPD应在距幽门至少2 cm位置离断十二指肠。对于恶性肿瘤,保留幽门者建议术中行十二指肠切缘的快速冰冻病理检查,保证切缘的阴性,同时需注意对幽门上下淋巴结(第5、6组)的清扫,并注意对胃大、小弯血管弓的保护。对于不保留幽门的LPD,胃离断方法同远端胃切除术,推荐使用腔镜下直线切割闭合器断胃,合理选择钉仓高度,减少断端出血。
(3)解剖肝十二指肠韧带
在胰颈上缘解剖、悬吊肝总动脉,清扫肝总动脉、肝固有动脉周围淋巴结;在排除或保护变异肝动脉后,于根部夹闭、离断胃十二指肠动脉和胃右动脉,必要时在其根部予以缝扎,以减少术后假性动脉瘤的发生。清扫淋巴结至肝门板处。切除胆囊,自胆囊管和肝总管汇合水平以上离断胆管。推荐术中快速冰冻切片明确胆道切缘状态。清扫门静脉前壁淋巴结,在门静脉悬吊和充分暴露下清扫其后方淋巴结。
(4)离断胰腺
分离胰颈下缘,明确肠系膜上静脉和门静脉位置,建立胰后隧道。胰后隧道建立困难者,无需强行建立。采用悬吊带或在胰腺下缘缝扎悬吊胰颈后以超声刀、剪刀或其他能量器械离断胰腺。推荐使用剪刀离断胰管,其有利于进行胰腺吻合。胰腺断面仔细止血。常规行胰腺切缘术中快速冰冻切片病理学检查,保证胰腺切缘的阴性。
(5)离断空肠
提起横结肠,确定空肠和屈氏韧带位置,距屈氏韧带10~15 cm处离断空肠。紧贴空肠游离至屈氏韧带左侧缘,注意保护肠系膜下静脉。将游离的空肠近端自小肠系膜根部后方置于胰头十二指肠后方。推荐选择合适高度钉仓的腹腔镜下直线切割闭合器离断空肠。
(6)解剖肠系膜上静脉-门静脉系统
沿横结肠系膜根部解剖探查肠系膜上静脉,仔细钳夹、离断右副结肠血管。从十二指肠第3段上缘处,沿肠系膜上静脉右侧壁自下而上逐步结扎、离断胃结肠静脉干(Henle干)、胰十二指肠下静脉、胰十二指肠上静脉、胃右静脉等属支,必要时结扎、离断汇入门静脉的胃冠状静脉。也可将肠系膜上静脉、门静脉悬吊后再行上述静脉分支的离断和淋巴结清扫。对肿瘤侵犯肠系膜上静脉或门静脉的患者,可据受累范围按照开腹手术方式完成血管切除与重建。
(7)解剖肠系膜上动脉-腹腔干系统
将肠系膜上静脉和门静脉系统悬吊、游离后,探查、分离肠系膜上动脉,钳夹、离断从肠系膜上动脉或空场动脉第一支发出的胰十二指肠下动脉,清扫肠系膜上动脉右侧180°的神经、淋巴结及结缔组织,自下而上清扫至肠系膜上动脉根部。探查显露腹腔干后,离断胰腺钩突与肠系膜膜上动脉及腹腔干根部之间的神经、淋巴结及结缔组织。
(8)胰腺吻合
胰肠吻合方式多种多样,基本原则是粘膜对粘膜、缝合严密、张力适度(详见本文技术改良之胰肠吻合)。胰管对空肠黏膜或其改良方式是当前LPD的主要吻合方法,胰管内常规放置支架管,具体的吻合方式可据腹腔镜下操作特点和术者开腹吻合的经验进行选择。
对于胰管扩张显著、腹腔镜下置管没有难度的病例建议腹腔镜下胰管空肠吻合;对胰管不扩张张、腹腔镜下难以置管者采取套入式胰肠吻合。
(9)胆肠吻合
胆肠吻合可采用连续缝合、间断缝合及连续间断相结合的方法。推荐使用可吸收倒刺线进行胆肠吻合。
(10)胃肠吻合
胃肠吻合方式主要包括腹腔镜下全手工缝合和直线切割闭合器进行胃后壁与空肠的侧侧吻合,术者可根据自身经验选择。
(五)腹腔镜胰十二指肠切除术中转开腹指征
LPD手术难度高、风险大、学习曲线长,为保障病人生命安全,手术过程中必要时要及时中转开腹,以免导致灾难性的结果。开腹手术是LPD的继续,是LPD的最终保障。
依据2017《腹腔镜胰十二指肠切除手术专家共识》,LPD出现以下情况应及时中转开腹:
1、恶性肿瘤侵犯胰头区域外且在腹腔镜下难以明确切除范围;
2、出血难以在腹腔镜下控制;
3、患者难以耐受气腹;
4、腹腔镜下病灶显露困难;
5、手术区域因严重慢性炎症导致腹腔镜下切除极为困难;
6、血管侵犯范围大难以在腹腔镜下完成血管重建;
7、腹腔镜下消化道重建困难或无法完成;
实践中,LPD中转开腹的指征并不局限于上述指征,出现任何影响手术安全和手术顺利进行的情况均需中转开腹。学界认识基本一致,术中发生难以控制的大出血及严重粘连影响手术正常是中转开腹的最主要指征。
张继红医生提示:最值得重视的是术中大出血的应急处理问题。手术团队要坚持“生命安全第一,微创手术第二”原则。术前做好应急止血和中转开腹的充分准备,术中迅速妥善处理意外大出血;不建议没有OPD经验的医生主刀LPD。
手术前:在进行LPD前要做好随时开腹手术的充分准备;要做好腹腔镜下和开腹手术时止血器械的充分准备,包括腹腔镜下哈巴狗血管钳、无创钳、腹腔镜血管缝合针线及持针器等腹腔镜下止血器械的准备和包括开腹下无创血管钳、血管缝合针线及持针器等手术止血器械的准备,避免发生难以控制的大出血时惊慌失措。
手术中:LPD术中,一旦发生难以控制的大出血,应当机立断在暂时控制大出血的前提下立即中转开腹。难以控制的大出血通常来源于肠系膜上静脉及门静脉的意外损伤,这时如有门静脉和肠系膜上静脉预置阻断带(悬吊带),可以轻提阻断带用哈巴狗血管钳阻断损伤血管两侧血流,立即开腹用血管外科器械进行缝合止血;如没有预置门静脉和肠系膜上静脉阻断带的情况下发生意外大出血,应用无创钳包括肠钳压迫或阻断门静脉或肠系膜上静脉和脾静脉以阻止或减少出血,迅速开腹止血;在无创钳无法阻断出血的情况下可用它压迫出血处血管两侧,用长针线缝合出血血管周围收紧但不打结以临时止血,开腹仔细止血后拆除应急止血缝线或用无创血管钳阻断后拆除应急止血缝线后再仔细止血。
主要参考文献
1.中华医学会外科学分会胰腺外科学组等。腹腔镜胰十二指肠切除手术专家共识。中华外科杂志,2017,55(5): 335-339
2.华杰,王巍。腹腔镜胰十二指肠切除术手术入路选择及评价。中国实用外科杂志,2022,42(5):513-518
