什么样的肝癌能够手术切除?
原发性肝癌是严重威胁病人生命安全的恶性肿瘤,生长快,发现晚,治疗效果差,预后不良。病理上分为肝细胞癌、胆管细胞癌、混合细胞癌三种类型。通常所说的肝癌是肝细胞癌的简称,胆管细胞癌又称肝内胆管癌。过去认为,射频消融和经肝动脉栓塞化疗(TACE)对早期肝癌可以获得和手术治疗相似的效果。随着新型治疗药物的问世和治疗理念的更新,肝癌综合治疗进入全新时代。以靶向、免疫治疗为代表的系统治疗,以介入、放疗为代表的非手术局部治疗,以及系统治疗和局部治疗的联合治疗,显著提高了肝癌治疗有效率,为患者带来希望。到目前为止,循证医学研究表明,外科手术仍然是肝癌最主要的根治性治疗方式,是使病人获得长期生存的最佳治疗方法。腹腔镜或机器人肝切除术成为肝切除术主流。然而,并非所有的肝癌都能手术切除,大多数肝癌患者就诊时就已经处于相对晚期而不能进行手术切除。许多病人和家属经常会问:什么样的肝癌能够手术切除?
要回答这个问题,必须从手术切除的彻底性和安全性两方面加以考量。简单地讲,肝癌是否可以切除,需要回答肝癌能否完整切除和切除后病人能否获得较长生存时间?肿瘤太大、太多,不能彻底切除或切除后病人直接面临肝功能衰竭甚至死亡,显然就不能切除;肿瘤虽小,但合并严重肝硬化,切除后肝脏功能不能代偿,病人仍然会会死于肝功能衰竭,也不能切除;肝癌局部情况适合切除,但病人由于全身情况差或心肺功能不佳,不能耐受手术,也不能手术切除。既能彻底切除肿瘤,切除后又能保证病人生命安全的肝癌是可以切除的肝癌。评估肝癌切除的彻底性和安全性就是明确病人有无手术切除指征(手术适应证和禁忌证)。
一、肝切除术的基本原则和评估方法
如何评估肝癌切除的彻底性和安全性?依据《原发性肝癌诊疗指南(2024版)》,肝癌手术切除的基本原则包括:(1)彻底性:完整切除肿瘤,切缘无残留肿瘤。(2)安全性:保留足够体积且有功能的肝组织(具有良好血供以及良好的血液和胆汁回流)以保证术后肝功能代偿,减少手术并发症、降低病死率。基于此,能够按照上述基本原则行手术切除的肝癌患者被认为是适合手术切除的患者,反之则不适合手术切除。
因此,肝癌手术切除指征(手术适应证)需从三个方面考虑:
1、病人全身情况能够耐受手术
病人一般情况良好,心肺肾功能代偿良好,无凝血机制障碍。
2、肝脏储备功能良好
术前应用肝功能Child-pugh评分、肝脏排泄试验(吲哚箐绿排泄试验,即ICG)、肝脏硬度测定、剩余肝脏体积测量等方法评估肝脏储备功能,预测肝切除术后不致于发生肝功能衰竭。
基本条件是:肝功能Child-pugh A级或Child-pugh B级经过短期治疗达到A级,肝脏排泄功能(ICGR15)正常范围或至少<20-30%,残肝体积能够代偿(正常肝脏剩余肝体积不低于标准肝体积30%,肝硬化肝脏剩余肝体积不低于标准肝体积40%)。实践中,常采取正常肝脏剩余肝体积不低于标准肝体积40%、肝硬化肝脏剩余肝体积不低于标准肝体积50%的标准,能更好地保障病人术后肝功能恢复。
3、肝癌能够彻底切除
基本条件是无远处转移,可行完整切除肝癌。
二、哪些肝癌适合手术切除?
根据《指南》,肝癌肝切除有可切除和潜在可切除肝癌。可切除肝癌首选肝切除术,潜在可切除肝癌进行转化治疗后达到彻底性和安全性原则后可行手术切除。
(一)首选肝切除的可切除性肝癌
依据《指南》,肝癌的外科治疗是肝癌患者获得长期生存的重要手段(证据等级2,推荐A),主要包括肝切除术和肝移植。中晚期肝癌(CNLCⅡb、Ⅲa、Ⅲb期)手术后总体生存虽然不令人满意,但当前系统抗肿瘤治疗与综合治疗取得长足进步,局部治疗和/或系统抗肿瘤治疗控制肿瘤的效果可以为中晚期肝癌患者提高手术切除率、降低术后复发转移和改善预后提供更多可能(证据等级4,推荐B),手术适应证适度扩大成为共识。因此,张继红医生认为,有《指南》上手术适应证的肝癌应首选手术治疗。
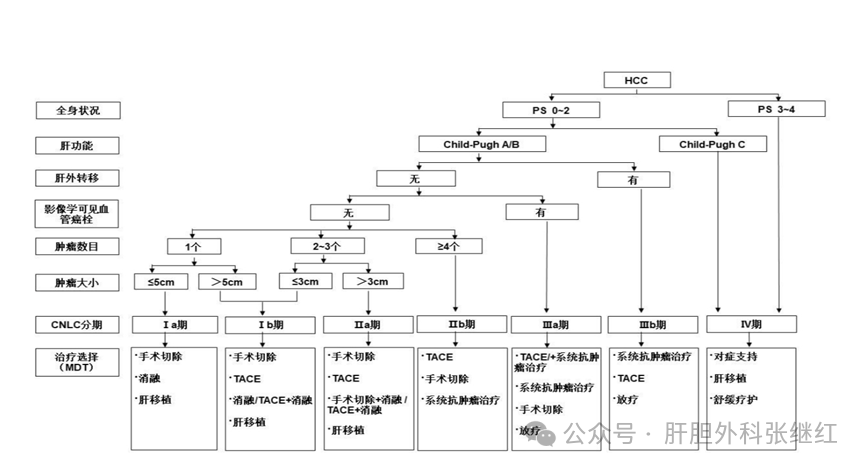
根据中国肝癌临床分期(CNLC分期,如上图),从CNLCⅠa期到CNLC Ⅲb期肝癌符合肝癌切除彻底性和安全性原则者均有肝切除适应证。首选肝切除的具体适应证包括:
(1)肝脏储备功能良好的CNLCⅠa期、Ⅰb期和Ⅱa期肝癌的首选治疗方式是手术切除(即使对于直径≤3cm的肝癌和复发性肝癌,手术切除也优于射频消融(证据等级2,推荐B)。
(2)CNLCⅡb期肝癌患者,如果肿瘤局限在同一段或同侧半肝者,或可以同时行术中消融处理切除范围外的病灶;即使肿瘤数目>3个,经过MDT讨论,手术切除有可能获得比其他治疗更好的效果,也可以推荐行手术切除(证据等级2,推荐B)(多数情况以TACE为主的非手术治疗为首选)。
(3)CNLC Ⅲa期肝癌,如符合以下情况,经过MDT讨论,也可考虑行手术切除[与索拉非尼相比,肝切除术治疗晚期非转移性肝癌的总体生存率(OS)和无进展生存时间(progression-free survival,PFS)显著更优]:
①合并门静脉分支癌栓(程氏分型Ⅰ/Ⅱ型)者,若肿瘤局限于半肝或肝脏同侧,可以考虑手术切除肿瘤同时切除癌栓,术后再实施TACE治疗、门静脉化疗或其他系统抗肿瘤治疗(证据等级3,推荐C);此类患者术前接受三维适形放射治疗,亦可以改善术后生存(证据等级2,推荐B);
②合并胆管癌栓但肝内病灶亦可以切除者;
③部分肝静脉受侵犯但肝内病灶可以切除者。
(4)伴有肝门部淋巴结转移者(CNLC Ⅲb期), 经过MDT讨论,可以考虑切除肿瘤的同时行肝门淋巴结清扫或术后外放射治疗;周围脏器受侵犯可以一并切除者,也可以考虑手术切除(CNLCⅢa期肝癌,大多数情况下不宜首选手术切除,尤其是合并门静脉主干癌栓者,而肝动脉栓塞化疗(transarterial chemoembolization,TACE)或TACE联合系统抗肿瘤治疗为主的非手术治疗为首选)。
(二)转化治疗成功后可切除的潜在可切除肝癌
依据《指南》和《原发性肝癌转化及围手术期治疗中国专家共识(2024版)》,转化治疗指不适合手术切除的肝癌患者,经过干预后获得适合手术切除机会,干预手段主要包括有功能的有功能的剩余肝脏体积 (future liver remnant,FLR)转化和肿瘤学转化。对于潜在可切除肝癌患者进行转化治疗转化为可切除肝癌,再进行以手术切除为主的多学科治疗,提高患者的术后生存。
1、有功能的剩余肝脏体积不足的转化
FLR转化是指针对有功能的FLR不足的肝癌患者,短期内增加有功能的FLR。其具体方式包括 (associating liver partition and portal vein ligation for staged hepatectomy,ALPPS)、门静脉栓塞术(portal vein embolization,PVE),ALPPS 较 PVE 具 有较高的转化效率(证据等级2,推荐A)。
2、肿瘤学转化
(1)系统抗肿瘤治疗在肿瘤学转化中的应用
抗血管生成药物联合ICIs是肝癌转化治疗的重要手段(证据等级 3,推荐 A)。建议在 MDT 框架下,关注肿瘤缓解的持续时间和缓解程 度,密切观察系统抗肿瘤治疗的毒性及其对转化后 手术切除的可能影响(证据等级3,推荐B)。
(2)经动脉介入治疗在肿瘤学转化中的应用
①TACE
TACE是针对中晚期不可切除肝癌常用的治疗方法,也是有效的肝癌转化传统治疗手段。
采用精细TACE以提高ORR,同时应适当控制TACE次数,避免多次TACE引起肝功能 损害。TACE与其他局部治疗或系统抗肿瘤治疗 的联合应用可以进一步提高转化率(证据等级 2, 推荐A)。
②肝动脉灌注化疗
对于肿瘤负荷较大或合并门静脉癌栓不可手术切除的肝癌患者,肝 动 脉 灌 注 化 疗 (hepatic arterial infusion chemotherapy,HAIC)具有较高的ORR和转化率(证据等级 2,推荐 B)。目前HAIC治疗推荐的化疗方案为 FOLFOX,通常需要连续完成≥4次的疗程。在 HAIC 基础上联合靶向和(或)免疫治疗,可以进一步提高转化率(证据等级 2,推荐B)
③放射治疗在肿瘤学转化中的应用
依据《共识》,在其他局部治疗、系统抗肿瘤治疗的基础上,联合放射治疗,可以进一步提高转化治疗 成功率(证据等级3,推荐B)。
转化治疗的意义在于使患者获得手术切除的机会,继而获得较长的无瘤生存时间及OS,缩短药物维持治疗的时间。手术切除是转化成功后患者获得长期 生存的重要手段。手术切除不仅可以消灭潜在残留肿瘤细胞,且术后病理学检查可为后续辅助治疗提供指导意见(证据等级3,推荐A)。
3、转化成功后手术切除的时机
(1)基于肿瘤反应选择合适的手术时机
转化成功的标志不仅在于是否适合手术切除,还应评估肿瘤缓解程度,后者与术后复发和长期生存更为相关(证据等级3,推荐B)。转化治疗使肿瘤达到客观缓解(缩瘤或者降期)或保持病灶稳定一段时间(如3-4个月),可能是切除后获得较好抗肿瘤学效果的前提条件。
(2)基于安全性选择合适的手术时机
手术安全性是转化切除前评估的重要内容,不仅需评估通常肝切除手术必备的安全性 检查项目,还需重点评估前期转化治疗对肝脏造成 的潜在影响。手术前,小分子靶向药物建议停药>1周,PD‑1/PD‑L1单抗建议停药>2周,贝伐珠单抗 建议停药>4 周;若行 TACE,需在末次 TACE 治疗 4周后进行手术;门静脉主干癌栓放疗与肝切除手 术之间的时间间隔通常为8周(证据等级4,推荐B)。
