如何判断胰腺肿块的良恶性?
胰腺肿块包括良性肿块和恶性肿块,其治疗方法和预后大相径庭。因此,发现胰腺肿块,首先应该明确其良恶性。那么,临床上怎样才能明确胰腺肿块是良性肿块还是恶性肿块呢?综合病史、临床表现、实验室检查和影像学检查可以基本明确诊断,但最后确诊依靠病理学诊断。临床医生多侧重于应用影像学表现判断胰腺肿块的良恶性,张继红医生编了一个顺口溜帮助广大医生和病员理解、记忆影像学诊断的奥秘:位置大小数轮现,性质钙化胰管关,包膜边界侵血管,淋巴器官转移见?欲知详情如何,且看下文分解。
1、年龄性别特点
胰腺实性-假乳头状瘤(SPN)好发于年轻女性;黏液性囊腺瘤(MCN)、浆液性囊腺瘤(SCN)以50~60岁女性高发,分别占99.8%和80%。(记忆要点:年轻女性假乳头,五十六十囊腺瘤)。
胰母细胞瘤主要发生在10岁以下男童;肿块型胰腺炎(MFP)以中青年男性居多;胰腺导管上皮癌(PDAC)、自身免疫性胰腺炎(AIP)、导管内乳头状黏液性肿瘤(IPMN)和胰腺转移瘤则以中老年男性居多。
胰腺神经内分泌肿瘤(PNEN)发生在60岁左右,如果为功能性肿瘤,则会更年轻,男女比例约1:1。
2、病史特点
慢性胰腺炎(CP)患者通常具有大量吸烟、饮酒史。
当患者出现多种肿瘤或与多发神经内分泌肿瘤I型(MEN)相关性较高的单一肿瘤或表现时,如垂体泌乳素瘤、甲状旁腺功能亢进,需要怀疑MEN I型可能。
当患者胰腺肿瘤同时伴发马方综合征或甲状腺髓样癌时,要考虑MEN II型可能。
当患者伴有颅内血管母细胞瘤和视网膜、肾脏、肾上腺、附睾等多脏器病变时,要考虑VHL(von Hippel–Lindau)综合征的可能。
3、症状学特征
早期出现症状、有恶液质表现者多为恶性肿块;症状不明显或肿块巨大时才出现症状通常为良性肿瘤可能性大。
胰头肿块可致胆道梗阻和梗阻性黄疸,但因肿块性质不同,胆道梗阻发生、发展的规律有所差别。进行性加重的梗阻性黄疸以胰头癌和胆管下段癌多见。慢性梗阻、胆总管扩张明显、胆红素不升高或轻度升高以良性肿块多见。
急性胰腺炎后无菌性胰腺坏死者可出现胆道梗阻和黄疸,但存在波动性。
其他肿瘤如良性内分泌肿瘤、低度恶性黏液性肿瘤常不伴胆道梗阻。
肿块型慢性胰腺炎常以上腹部发作性绞痛为特征,疼痛时常伴血清淀粉酶和脂肪酶升高。
胰腺癌在突破癌包膜前无明显症状或仅有上腹部不适、隐痛,当肿瘤突破包膜发生浸润时,疼痛较重,以安静或夜间更明显。
导管内黏液性乳头状瘤或癌可因胰腺导管梗阻而发生急性胰腺炎导致上腹部疼痛。
内分泌肿瘤和其他低度恶性肿瘤如黏液性瘤或腺瘤等常无明显疼痛症状。
在发现肿块前数月出现血糖升高或诊断为糖尿病,肿块多为恶性。但在长期糖尿病基础上发生的胰腺肿块,应注意炎症性改变。
无症状或症状不典型患者就诊:通常于体检时无意发现,或仅伴有轻微的腹痛、腹部肿块,而其它临床和化验血指标均正常,多为良性病变可能性大,以SPTP、MCN、SCN、IPMN和无功能的PENP为主。
有典型临床症状就诊者:胰腺癌(PC)、MFP、AIP或胰腺其它占位压迫胰胆管的患者常以梗阻性黄疸就诊。Wipple三联征患者、空腹血浆胃泌素、胰高血糖素、生长抑素升高提示胰腺神经内分泌肿瘤。
4、血清学检查
(1)肝功能检查
提示阻塞性黄疸伴胰头肿块者多为恶性肿瘤;胰头肿块较大而无梗阻性黄疸者多为良性肿块。
(2)免疫指标
血清IgG4或其它少见免疫学指标增高提示自身免疫性胰腺炎。
(3)肿瘤标志物
胰腺恶性肿瘤患者通常CA19-9、CA242、CA50、CEA等癌性指标增高。
CA19-9正常,AFP升高提示胰腺腺泡细胞癌(ACCP)。
Wipple三联征患者、空腹血浆胃泌素、胰高血糖素、生长抑素升高提示胰腺神经内分泌肿瘤。
5、影像学检查
《中国胰腺癌综合诊治指南(2020版)》指出,影像学技术诊断胰腺癌的基本原则是:(1)完整 (显示整个胰腺);(2)精细(层厚 1-3 mm 的薄层扫 描);(3)动态(动态增强、定期随访);(4)立体(多轴面重建,全面了解胰腺周围毗邻关系)。通过B超、CT或MRI等影像学检查,明确病变的形态学特征,区别恶性胰腺占位或良性占位,结合肿瘤学标志物检测进一步明确胰腺肿块的良恶性。
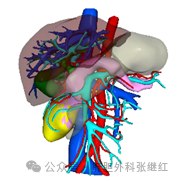
超声内镜(准确性,(endoscopic ultrasonography,EUS)对判断胰腺肿块及是否浸润有较高准确性。EUS及 其 引 导 下 的 细 针 穿 刺 活 检(fine needle aspiration,FNA)是目前胰腺癌定位和定性诊断最准确的方法。
胰腺CT增强一般采用三期扫描:动脉期、胰腺实质期和门脉期。动脉期胰腺实质强化不明显,主要评估肿块周围的重要动脉,胰腺实质期可以获得正常胰腺组织和肿块间的最佳对比度,最后是门脉期,此期正常胰腺实质内造影剂基本退出,如果此期仍可见局灶性强化多数提示为纤维组织的延迟强化,此期也适用于评估肝脏转移。三维动态增强扫描类同于多期增强CT,能清晰显示病灶血供特点以及与周围结构的关系,必要时可以三维成像。
MRI对胰腺肿块的独特优势是软组织对比优于CT。在显示囊液性成分、胰胆管和病灶内出血方面优于CT。脂肪抑制技术减少了相位伪影,增加了胰腺信号强度。磁共振胰胆管成像(magneticresonance cholangiopancreatography,MRCP)显示较小的囊性病变及病变与胰管间的关系方面优于MSCT,它的效能等同于逆行性胰胆管造影(endoscopic retrograde cholangiopancreatography,ERCP)。多种弥散加权成像技术(DWI、IVIM、DKI等),在显示病灶的异质性方面具有较大潜能。
正电子发射断层显像/X 线计算机体层成像 (positron emission tomography‐computed tomography, PET‐CT)或 PET‐MRI 可显示肿瘤的代谢活性和代 谢负荷 ,在发现胰外转移、评价全身肿瘤负荷方面具有明显优势。
晚期胰腺癌表现为肿块边界不清的低密度改变,可能浸润胰周或包绕胰周血管。局限于胰腺内的癌性肿块表现为边界不清的低密度改变,可致胆管或(和)胰管梗阻性改变。内分泌肿瘤表现为边界较清楚的实性肿块。黏液性和浆液性腺瘤表现为边界清楚的低密度肿块。慢性胰腺炎肿块常伴胰管扩张和结石,甚至胰内潴留性囊肿,糖尿病引起的胰腺炎性肿块在影像学上难与胰腺癌鉴别,但癌抗原19-9(CA 19-9)常不升高或轻度升高。急性胰腺炎后无菌性胰腺坏死表现为胰头低密度灶,但患者近期或近年有急性胰腺炎病史。
陆建平等在《基于多学科协作的胰腺肿块诊断思路》[放射学实践,2017,32(9):909-917]一文中将胰腺占位分为肿瘤性占位和非肿瘤性占位,肿瘤占位包括实性、囊实性、囊性肿块,并将胰腺肿块的诊断思路总结如下图。
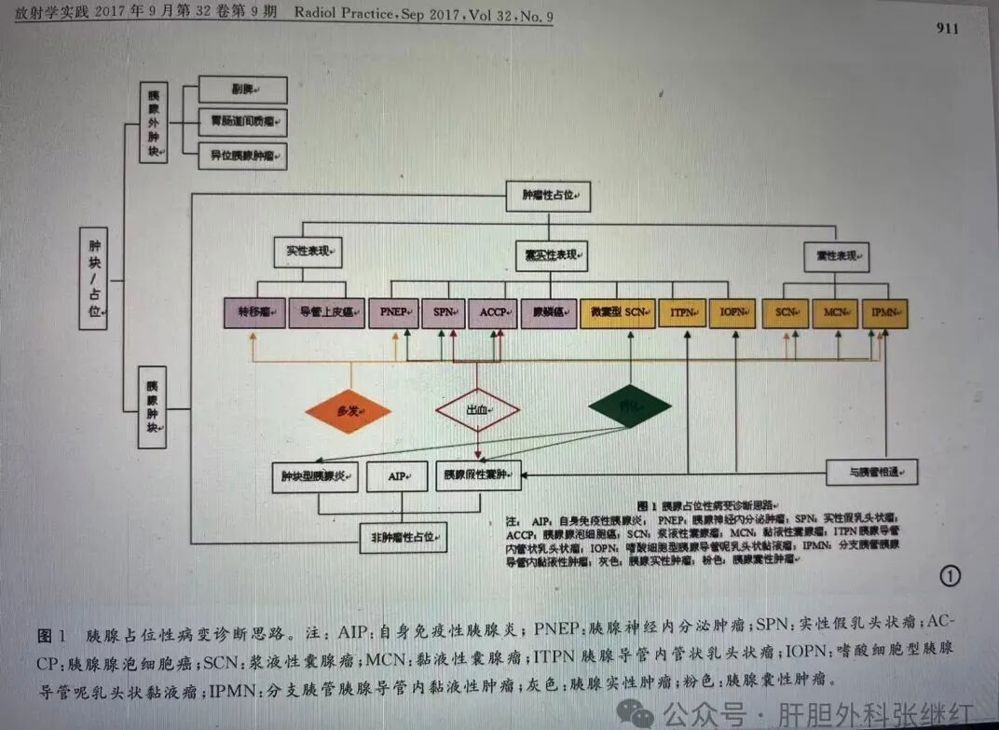
综合文献资料,从影像学上依据胰腺肿块的位置、大小、数量、性质、边缘和包膜、胰管扩张及程度、累及范围和转移情况,基本可以对胰腺癌的良恶性作出综合性判断(记忆顺口溜:位置大小数轮现,性质钙化胰管关,包膜边界侵血管,淋巴器官转移见?)。
(1)肿块的位置、大小、数量和胰腺轮廓(位置大小数轮现)
PDAC、MFP和SCN均以胰头部多见,分支型IPMN以钩突多见,MCN多发生于胰体尾部。
胰腺肿块基本以单发为主,多灶性肿块并不多见,主要发生在MEN I型和II型、分支胰管型IPMN、VHL和胰腺转移瘤。
胰腺肿块的良恶性与病灶发现时的大小有较大的相关性。肿块体积较小、胰腺轮廓五明显改变,多为良性;肿块体积较大、胰腺轮廓改变明显则多为恶性。直径>2 cm的肿瘤常常突出于胰腺,使其轮廓变形,胰腺各部分比例失调,肿块上游胰腺常常萎缩。
位于胰头部肿块,由于其生长空间狭小,较易引起胰胆管梗阻,所以发现时肿块体积一般较小。
对于恶性度较高或有功能的胰腺肿瘤(如PC、功能性PNEN)往往发现时体积较其它胰腺占位直径小。无功能PNEN、SPN、ACCP体积变化较大,可以从数毫米至十几厘米不等,与偶然的影像体检相关,也可能与肿瘤乏嗜神经现象有关。炎性肿块轮廓较光整,无分叶,平扫时与正常组织成等密度或等高混杂密度,钙化多见,成砂粒样或斑片状钙化;动脉期轻度强化(纤维组织增生),病灶呈相对低密度,门静脉期逐渐强化。胰头癌围绕主胰管呈浸润性生长,胰头增大变形,边缘呈分叶状,与正常胰腺分解不清,多成等密度或等低混合密度,液化坏死多见,钙化少见;胰头癌为少血供无包膜实质肿瘤,强化程度弱、速度慢,动脉期表现为不均匀低密度灶,与周围血供丰富的胰腺组织迅速强化形成鲜明对比。
(2)肿块性质:胰腺肿块分为实性、囊性和囊实性肿块,其中有恶性、良性与真性、假性之别。恶性肿块常有坏死液化,密度多有不均匀,轮廓欠规则,增强扫描不均匀强化;良性肿块一般密度均匀,轮廓规整,增强扫描炎性肿块均匀强化。真性囊肿壁薄,影像学上经常不能显示囊壁;一个光滑的壁厚大囊性肿块是假性囊肿的体征。(性质)
(3)钙化:恶性肿块很少钙化,除非发生在已有钙化的慢性胰腺炎基础上。炎性病变常有钙化,以肿块型胰腺炎和胰腺假性囊肿最多见。ACCP大约有30%左右的钙化,这是与PDAC的重要鉴别点。SCN的钙化多发生在肿块中心的星芒状疤痕上(10%)。MCN则以囊壁钙化更常见,MCN出现囊内间隔的不规则增厚和钙化提示肿瘤恶变。(钙化)
(4)肿块与胰管的关系及胰管扩张形态:肿块与胰管的关系可分为与胰管相通和不相通。在MRCP或沿着主胰管方向进行曲面重建,大部分胰腺肿块可以明确与胰管之间的关系。当肿块与胰管不相通时,常对胰管产生浸润性和(或)外压性影响。PDAC对胰管浸润常表现为肿块处突然截断,并继发上游胰管扩张,扩张的上游胰管多呈平滑连续性,胰头癌常同时合并软藤状扩张的胆总管,出现典型的“双管征”。其余胰腺肿块对胰管产生的影响以外压性改变为主。与胰管相通的病变主要有IPMN、ITPN和PPC。恶性肿块胰管扩张可呈光滑、串珠状,慢性炎症使胰管呈不规则扩张;胰管扩张与胰腺实质厚度之比大于0.5为恶性可能性大,小于0.5为良性可能性大。(胰管关)
(5)包膜和边界:肿块侵袭性越强则与周围分界越不清楚。而肿块的包膜也是与周围组织分界是否清楚的主要原因之一,包膜的存在与否、完整与否均提示着肿瘤的恶性程度。通常恶性度高的肿瘤因其浸润性生长而无包膜(如PDCA);当包膜不完整或者原本完整的包膜出现不完整,说明肿瘤突破包膜呈浸润性生长,提示肿瘤发生恶变。(包膜边界)
(6)血管侵犯:恶性肿瘤侵犯血管或包埋血管;良性肿块不侵犯血管,无包埋血管现象,最多是挤压血管。CT原始横断面薄层图像进行多种三维后处理,显示肿块与周围脏器的空间关系,特别是与周围重要血管之间的关系,能对肿块进行分期和切除性评价,成为胰腺肿块的首选影像方法。(侵血管)
(7)淋巴结肿大:恶性肿瘤较早转移到腹腔动脉或肠系膜上动脉周围淋巴结;(淋巴)
(8)邻近器官变化与转移灶:慢性胰腺炎使肾前筋膜或肾周筋膜增,胰腺癌很少出现肾周筋膜增厚;胰腺癌出现“双管征、不相交”,慢性胰腺炎无此现象;肝转移、邻近器官和腹膜侵犯等为恶性肿块特征。(器官转移见?)
6、病理学诊断
目前获得组织病理学或细胞学标本的方法包括:(1)超声、EUS 或 CT 引导下穿刺活检;(2)腹水脱落细胞学检查;(3)腹腔镜或开腹手术下探查活检。
术前病理诊断可行胰腺细针穿刺活检,技术要求较高。临床上多依赖于术中冰冻切片检查和术后病理诊断。
